อินดิเคเตอร์ คือ สารที่ใช้บอกความเป็นกรด-เบส ของสารละลายได้อย่างหนึ่ง สารประกอบที่เปลี่ยนสีได้ที่ pH เฉพาะตัว จะถูกนำมาใช้เป็นอินดิเคเตอร์ได้ เช่น ฟีนอล์ฟทาลีน จะไม่มีสีเมื่ออยู่ในสารละลายกรด และจะเปลี่ยนเป็นสีชมพู เมื่ออยู่ในสารละลายเบสที่มี pH 8.3

ภาพฟีนอล์ฟทาลีน
อินดิเคเตอร์สำหรับกรด-เบส เป็นสารอินทรีย์ อาจเป็นกรดหรือเบสอ่อนๆ ซึ่งสามารถเปลี่ยนจากรูปหนึ่งไปเป็นอีกรูปหนึ่งได้ เมื่อ pH ของสารละลายเปลี่ยน
การเปลี่ยนสีของ
HIn เป็นสัญลักษณ์ของอินดิเคเตอร์ที่อยู่ในรูปกรด (Acid form)
In- เป็นสัญลักษณ์ของอินดิเคเตอร์ที่อยู่ในรูปเบส (Basic form)
รูปกรดและรูปเบสมีภาวะสมดุล เขียนแสดงได้ด้วยสมการ ดังนี้
HIn (aq) + H2O (l) H3O+ (aq) + In- (aq)
ไม่มีสี * สีชมพู* ; (* = กรณีเป็นฟีนอล์ฟทาลีน)
(รูปกรด) (รูปเบส)
Kind = |
HIn และ In- มีสีต่างกันและปริมาณต่างกัน จึงทำให้สีของสารละลายเปลี่ยนแปลงได้ ถ้าปริมาณ HInมากก็จะมีสีของรูปกรด ถ้ามีปริมาณ In-มากก็จะมีสีของรูปเบส การที่จะมีปริมาณ HIn หรือ In มากกว่าหรือน้อยกว่านั้นขึ้นอยู่กับปริมาณ H3O+ ในสารละลาย ถ้ามี H3O+ มากก็จะรวมกับ In- ได้เป็น HIn ได้มากจะเห็นสารละลายใสไม่มีสีของ HIn แต่ถ้าอยู่ในสารละลายที่มี OH- มาก OH-จะทำปฏิกิริยากับ H3O+ ทำให้H3O+ ลดลง ซึ่งจะมีผลทำให้เกิดปฏิกิริยาไปข้างหน้าได้ In- มากขึ้น จะเห็นสารละลายในรูปของ In- คือเห็นเป็นสีชมพู
ช่วง pH ที่อินดิเคเตอร์เปลี่ยนสีจากรูปหนึ่งไปเป็นอีกรูปหนึ่ง สารละลายจะมีสีผสมระหว่างรูปกรดและรูปเบส เรียกว่า ช่วง pH ของอินดิเคเตอร์ (pH range หรือ pH interval)
ช่วง pH ของอินดิเคเตอร์หาได้จากค่า Kind ของอินดิเคเตอร์ดังนี้
HIn (aq) + H2O (l) H3O+ (aq) + In- (aq)
ไม่มีสี * (รูปกรด) สีชมพู* (รูปเบส) ; (* = กรณีเป็นฟีนอล์ฟทาลีน)
นั่นคือ ช่วง pH ของอินดิเคเตอร์ = pKind 1 หมายความว่า สีของอินดิเคเตอร์จะเริ่มเปลี่ยนแปลงเมื่อ pH = pKind 1 ซึ่งเป็นค่าโดยประมาณ แต่ถ้า [HIn] มากกว่าหรือน้อยกว่า [In- ] 10 เท่าขึ้นไป อาจถึง 100 เท่า ช่วง pH ของอินดิเคเตอร์ก็จะเปลี่ยนไป ช่วง pH ของอินดิเคเตอร์ที่ถูกต้องจริงๆ ของแต่ละอินดิเคเตอร์หาได้จากการทดลอง
ตัวอย่างเช่น เมทิลเรด มีช่วง pH 4.4 - 6.2 หมายความว่า สารละลายที่หยดเมทิลเรดลงไป จะเปลี่ยนสีจากรูปกรด (แดง) ไปเป็นรูปเบส (เหลือง) ในช่วง pH ตั้งแต่ 4.4 - 6.2 นั่นคือ
- ถ้า pH < 4.4 จะให้สีแดง (รูปกรด)
- pH อยู่ระหว่าง 4.4 - 6.2 จะให้สีผสมระหว่างสีแดงกับเหลือง คือ สีส้ม
- pH > 6.2 จะให้สีเหลือง (รูปเบส)
สีของอินดิเคเตอร์แต่ละชนิด จะเปลี่ยนในช่วง pH ที่ต่างกัน ซึ่งแสดงได้ดังภาพ
อย่างไรก็ตาม อินดิเคเตอร์ชนิดหนึ่งๆ จะใช้หาค่า pH ของสารละลายได้อย่างคร่าวๆ เท่านั้น เช่น เมื่อนำสารละลายมาเติม เมทิลออเรนจ์ลงไป (ช่วง pH ของเมทิลออเรนจ์เท่ากับ 3.0 - 4.4 และสีที่เปลี่ยนอยู่ในช่วง สีแดง เหลือง) ถ้าสารละลายมีสีเหลืองหลังจากหยดเมทิลออเรนจ์ แสดงว่าสารละลายนี้มี pH ตั้งแต่ 4.4 ขึ้นไป ซึ่งอาจมีฤทธิ์เป็นกรด กลางหรือ เบส ก็ได้ ดังนั้น การหาค่า pH ของสารละลายหนึ่งๆ อาจจะต้องใช้อินดิเคเตอร์หลายๆ ตัว แล้วนำข้อมูลมาวิเคราะห์ pH ของสารละลายร่วมกัน
ตัวอย่าง การทดลองหาค่า pH ของสารละลายชนิดหนึ่ง โดยใช้อินดิเคเตอร์ 5 ชนิดด้วยกัน ผลการทดลองเป็นดังนี้
ชนิดของอินดิเคเตอร์ | ช่วง pH | สีที่เปลี่ยน | สีสารละลายที่ได้จากการทดลอง |
1. methyl yellow 2. Bromeresol green 3. Methyl red 4. Bromothymol blue 5. Phenophtalein | 2.9-4.0 3.8-5.4 4.4-6.2 6.0-7.6 8.0-9.6 | สีแดง-เหลือง เหลือง-น้ำเงิน แดง-เหลือง เหลือง-น้ำเงิน ไม่มีสี-สีชมพู | เหลือง น้ำเงิน ส้ม เหลือง ไม่มีสี |
ให้หาค่า pH ของสารละลายจากข้อมูลการทดลองข้างต้น
แนวคิด จากอินดิเคเตอร์ชนิดที่ 1 แสดงว่า pH ของสารละลาย > 4 จากอินดิเคเตอร์ชนิดที่ 2 แสดงว่า pH ของสารละลายอยู่ระหว่าง 4.4-6.2 จากอินดิเคเตอร์ชนิดที่ 3 แสดงว่า pH ของสารละลาย > 5.4 จากอินดิเคเตอร์ชนิดที่ 4 แสดงว่า pH ของสารละลาย < 6 จากอินดิเคเตอร์ชนิดที่ 5 แสดงว่า pH ของสารละลาย < 8.0 สรุปได้ว่า สารละลายมี pH อยู่ระหว่าง 5.4 - 6
การหา pH ของสารละลายโดยใช้อินดิเคเตอร์หลายๆ ชนิดนี้ ไม่สะดวกในการใช้ จึงมีการคิดที่จะนำอินดิเคเตอร์หลายๆ ชนิด ซึ่งเปลี่ยนสีในช่วง pH ต่างๆ กันมาผสมกันในสัดส่วนที่เหมาะสม จะสามารถใช้บอกค่า pH ของสารละลายได้ละเอียดขึ้น อินดิเคเตอร์ผสมนี้เรียกว่า ยูนิเวอร์ซัลอินดิเคเตอร์ ซึ่งสามารถเปลี่ยนสีได้ในสารละลายที่มี pH ต่างๆ กันเกือบทุกค่า
การใช้ยูนิเวอร์ซัลอินดิเคเตอร์ หยดยูนิเวอร์ซัลอินดิเคเตอร์ลงในสารละลายที่ต้องการหาค่า pH ประมาณ 3 หยดต่อสารละลาย 3 cm3 สังเกตสีของสารละลายแล้วเปรียบเทียบกับสีมาตรฐานของยูนิเวอร์ซัลอินดิเคเตอร์ที่ pH ต่างๆ ว่าสีของสารละลายตรงกับสีมาตรฐานที่ pH ใด ก็จะมีค่าเท่ากับ pH นั้น
ตาราง การเปลี่ยนสีของสารละลาย เมื่อใช้ยูนิเวอร์ซัลอินดิเคเตอร์
pH สารละลาย | สี |
3 | แดง |
4 | ส้มแดง |
5 | ส้ม |
6 | ส้มเหลือง |
7 | เหลืองเขียว |
8 | เขียว |
9 | น้ำเงินเขียว |
10 | ม่วง |
11 | ม่วงแดง |
อินดิเคเตอร์กับการไทเทรตกรด-เบส
อินดิเคเตอร์กรด-เบส ที่เหมาะสมกับปฏิกิริยาการไทเทรตจะต้องมีค่า pH ที่จุดกึ่งกลางช่วงการเปลี่ยนสีใกล้เคียงหรือเท่ากับ pH ที่จุดสมมูลของปฏิกิริยา นอกจากนี้ การเลือกใช้อินดิเคเตอร์กรด-เบส ต้องพิจารณาสีที่ปรากฎ จะต้องมีความเข้มมากพอที่จะมองเห็นได้ง่าย หรือเห็นการเปลี่ยนสีได้ชัดเจน ช่วงการเปลี่ยนสีของอินดิเคเตอร์ จะเกิดขึ้นในช่วง 2 หน่วย pH
ตัวอย่างเช่น การไทเทรตกรดแก่กับเบสแก่ pH ของสารละลายผลิตภัณฑ์ที่เกิดจากปฏิกิริยาการไทเทรต เมื่อถึงจุดสมมูลมีค่าใกล้เคียง 7 ก็ควรเลือกใช้อินดิเคเตอร์ที่มีช่วง pH ของการเปลี่ยนสีใกล้เคียงกับ 7 เช่น อาจใช้โบรโมไทมอลบลูหรือ ฟีนอล์ฟทาลีน ซึ่งจะเปลี่ยนจากไม่มีสีเป็นสีชมพู ในช่วง pH 8.20-10.00 เป็นต้น ดังนั้น ถ้าทราบ pH ของสารละลายที่จุดสมมูลของปฏิกิริยาการไทเทรตก็สามารถเลือกอินดิเคเตอร์ที่ เหมาะสมได้
การเลือกอินดิเคเตอร์ ก็ขึ้นอยู่กับชนิดของปฏิกิริยาระหว่างกรดกับเบส เพราะที่จุดสมมูลของแต่ละปฏิกิริยานั้น มีค่า pH ที่ต่างกัน
ตัวอย่างเช่น การไทเทรตกรดแก่กับเบสแก่ pH ของสารละลายผลิตภัณฑ์ที่เกิดจากปฏิกิริยาการไทเทรต เมื่อถึงจุดสมมูลมีค่าใกล้เคียง 7 ก็ควรเลือกใช้อินดิเคเตอร์ที่มีช่วง pH ของการเปลี่ยนสีใกล้เคียงกับ 7 เช่น อาจใช้โบรโมไทมอลบลูหรือ ฟีนอล์ฟทาลีน ซึ่งจะเปลี่ยนจากไม่มีสีเป็นสีชมพู ในช่วง pH 8.20-10.00 เป็นต้น ดังนั้น ถ้าทราบ pH ของสารละลายที่จุดสมมูลของปฏิกิริยาการไทเทรตก็สามารถเลือกอินดิเคเตอร์ที่ เหมาะสมได้
การเลือกอินดิเคเตอร์ ก็ขึ้นอยู่กับชนิดของปฏิกิริยาระหว่างกรดกับเบส เพราะที่จุดสมมูลของแต่ละปฏิกิริยานั้น มีค่า pH ที่ต่างกัน
การฟของการไทเทรตจะช่วยในการเลือกอินดิเคเตอร์ที่เหมาะสมได้ดี เพราะกราฟจะแสดงค่า pH ของสารละลายขณะไทเทรต ตั้งแต่ก่อนจุดสมมูล ที่จุดสมมูล และหลังจุดสมมูล จุดที่ pH ของสารละลายเปลี่ยนแปลงมาก ซึ่งเป็นจุดสมมูลนั้น จะบอกช่วง pH ของอินดิเคเตอร์ที่จะเลือกใช้ ในการพิจารณาเลือกอินดิเคเตอร์ จากกราฟของการไทเทรต จะแบ่งออกตามชนิดของปฏิกิริยาดังนี้
1.อินดิเคเตอร์สำหรับปฏิกิริยาระหว่างกรดแก่กับเบสแก่
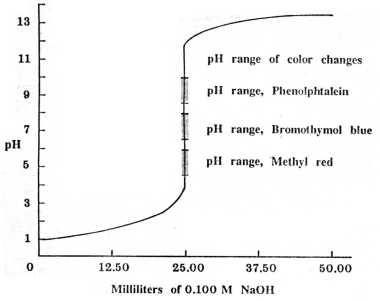
รูปกราฟของการไทเทรตระหว่างกรดแก่และเบสแก่ จะแสดง pH ที่จุดสมมูลอยู่ที่ pH ใกล้เคียง 7
จากกราฟ จะเห็นว่าค่า pH เปลี่ยนแปลงรวดเร็วที่จุดใกล้ๆ จุดยุติ (ตั้งแต่ pH 4-10) ดังนั้นอินดิเคเตอร์ที่มีช่วง pH ของการเปลี่ยนแปลงสีระหว่าง 4 ถึง 10 ก็สามารถนำมาใช้ได้ ซึ่งอินดิเคเตอร์ที่เหมาะสมที่อาจใช้ได้ ได้แก่ เมทิลเรด (4.4-6.2) โบรโมไทมอลบลู (6.0-7.5) และฟีนอล์ฟทาลีน(8.2-10.0) ดังแสดงในภาพ แต่เรามักจะนิยมใช้ฟีนอล์ฟทาลีน เพราะสังเกตการเปลี่ยนแปลงสีได้ชัดเจน สำหรับ โบรโมคลีซอล กรีน (3.8-5.4) ไม่เหมาะสมที่จะใช้เป็นอินดิเคเตอร์สำหรับกรดแก่และเบสแก่ เพราะช่วงเปลี่ยนสีที่เป็นรูปเบสของอินดิเคเตอร์ จะเกิดก่อนจุดสมมูล ทำให้เกิดความคลาดเคลื่อนในการบอกจุดยุติ
2.อินดิเคเตอร์สำหรับปฏิกิริยาระหว่างกรดอ่อนกับเบสแก่
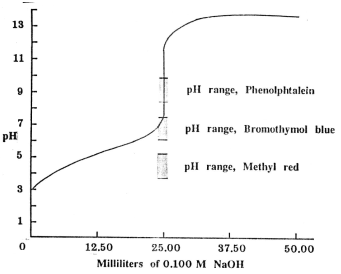
การเลือกอินดิเคเตอร์สำหรับการไทเทรตกรดอ่อน เช่น กรดแอซิติก กับเบสแก่ เช่น NaOH จะมีข้อจำกัดมากกว่าที่จุดสมมูลของการไทเทรต สารละลายจะมีโซเดียมแอซิเตต ทำให้สารละลายเป็นเบส มี pH มากกว่า 7
รูปกราฟแสดงการไทเทรตระหว่างกรดอ่อนกับเบสแก่และอินดิเคเตอร์ที่เหมาะสม
จากกราฟจะเห็นได้ว่า เมทิลเรด จะเปลี่ยนสีก่อนจุดสมมูลจึงไม่เหมาะที่จะใช้เป็นอินดิเคเตอร์สำหรับกรดแอซิติกกับ NaOH (เข้มข้น 0.100 M) ฟีนอล์ฟทาลีนเปลี่ยนสีที่ช่วงจุดสมมูลพอดี โบรโมไทมอลบลู อาจจะใช้เป็นอินดิเคเตอร์ได้ดี เมื่อใช้สีมาตรฐานเทียบ
3.อินดิเคเตอร์สำหรับปฏิกิริยาระหว่างกรดแก่กับเบสอ่อน
การเปลี่ยนแปลง pH ของสารละลายขณะไทเทรตเบสอ่อน เช่น NH3 กับกรดแก่ เช่น HCl จะค่อยๆ ลดลง เมื่อใช้ HCl เป็นสารมาตรฐาน ที่จุดยุติจะได้เกลือ NH4Cl และ pH < 7 ในการไทเทรต 0.100 M NH3 กับ 0.100 M HCl จะได้กราฟของการไทเทรต (ดังภาพ)
รูปกราฟของการไทเทรตระหว่าง 0.1000 M NH3 กับ 0.1000 M HCl
จากกราฟ เราสามารถพิจารณาช่วง pH 3-7.5 ในการเลือกอินดิเคเตอร์ ซึ่งเราอาจใช้โบรโมไทมอลบลูหรือเมทิลเรดได้ แต่ไม่ควรใช้ฟีนอล์ฟทาลีนเพราะช่วง pH ของฟีนอล์ฟทาลีนมากกว่า 7 ทำให้เกิดความคลาดเคลื่อนในการบอกจุดสมมูล

การทดสอบความเป็นกรด – เบสของสารละลาย
ความเป็นกรด - เบส หรือค่า pH ของสารละลายสามารถทดสอบได้โดยใช้อินดิเคเตอร์
อินดิเคเตอร์ที่ใช้ในการทดสอบความเป็นกรด - เบส หรือค่า pH ของสารละลายได้แก่
1. กระดาษลิตมัส มีสีแดงกับสีน้ำเงิน มีการเกิดขึ้น ดังนี้
- สารละลายกรด หรือสารละลายที่มีค่า pH ต่ำกว่า 7 จะเปลี่ยนสีของกระดาษลิตมัสจากสีน้ำเงินเป็นสีแดง แต่ไม่เปลี่ยนสีของกระดาษลิตมัสสีแดง
- สารละลายเบสหรือสารละลายที่มีค่า pH สูงกว่า 7 จะ เปลี่ยนสีของกระดาษลิตมัสจากสีแดงเป็นสีน้ำเงินแต่ไม่เปลี่ยนสีของกระดาษลิตมัสสีน้ำเงิน
- สารละลายเป็นกลางหรือสารละลายที่มีค่า pH เท่ากับ 7 จะไม่เปลี่ยนสีของกระดาษลิตมัสทั้งสีแดงและสีน้ำเงิน
2. สารละลายฟีนอล์ฟทาลีน เป็นอินดิเคเตอร์ที่ไม่มีสี เมื่อหยดสารละลายกรด สีของสารละลายจะคงเดิม เมื่อหยดสารละลายเบส สีของสารละลายฟีนอล์ฟทาลีนจะเปลี่ยนเป็นสีชมพูม่วง แต่ถ้าเป็นเบสแก่จะเปลี่ยนเป็นสีแดง
3. สารละลายยูนิเวอร์แซลอินดิเคเตอร์ เป็นการนำอินดิเคเตอร์หลาย ๆชนิดที่มีการเปลี่ยนสีในช่วง pH ต่างกันมาผสมกันในสัดส่วนที่เหมาะสม
จึงสามารถบอกค่าความเป็นกรด - เบส ของสารละลายโดยบอกค่า pH ที่ละเอียด และถูกต้องยิ่งขึ้น
ความเป็นกรด - เบส หรือค่า pH ของสารละลายสามารถทดสอบได้โดยใช้อินดิเคเตอร์
อินดิเคเตอร์ที่ใช้ในการทดสอบความเป็นกรด - เบส หรือค่า pH ของสารละลายได้แก่
1. กระดาษลิตมัส มีสีแดงกับสีน้ำเงิน มีการเกิดขึ้น ดังนี้
- สารละลายกรด หรือสารละลายที่มีค่า pH ต่ำกว่า 7 จะเปลี่ยนสีของกระดาษลิตมัสจากสีน้ำเงินเป็นสีแดง แต่ไม่เปลี่ยนสีของกระดาษลิตมัสสีแดง
- สารละลายเบสหรือสารละลายที่มีค่า pH สูงกว่า 7 จะ เปลี่ยนสีของกระดาษลิตมัสจากสีแดงเป็นสีน้ำเงินแต่ไม่เปลี่ยนสีของกระดาษลิตมัสสีน้ำเงิน
- สารละลายเป็นกลางหรือสารละลายที่มีค่า pH เท่ากับ 7 จะไม่เปลี่ยนสีของกระดาษลิตมัสทั้งสีแดงและสีน้ำเงิน
2. สารละลายฟีนอล์ฟทาลีน เป็นอินดิเคเตอร์ที่ไม่มีสี เมื่อหยดสารละลายกรด สีของสารละลายจะคงเดิม เมื่อหยดสารละลายเบส สีของสารละลายฟีนอล์ฟทาลีนจะเปลี่ยนเป็นสีชมพูม่วง แต่ถ้าเป็นเบสแก่จะเปลี่ยนเป็นสีแดง
3. สารละลายยูนิเวอร์แซลอินดิเคเตอร์ เป็นการนำอินดิเคเตอร์หลาย ๆชนิดที่มีการเปลี่ยนสีในช่วง pH ต่างกันมาผสมกันในสัดส่วนที่เหมาะสม
จึงสามารถบอกค่าความเป็นกรด - เบส ของสารละลายโดยบอกค่า pH ที่ละเอียด และถูกต้องยิ่งขึ้น
อินดิเคเตอร์ที่ใช้ในการทดสอบความเป็นกรด เบสของดินได้แก่
1. ยูนิเวอร์แซลอินดิเคเตอร์ เป็นตลับ ภายในมีกระดาษยูนิเวอร์แซลอินดิเคเตอร์ และบนตลับจะมีแผ่นเทียบสีค่า pH ตั้งแต่ 1 ถึง 14
ดินเป็นกรด จะเปลี่ยนสีกระดาษยูนิเวอร์แซลอินดิเคเตอร์จากสีน้ำตาลเป็นสีแดง
ดินเป็นเบส จะเปลี่ยนสีกระดาษยูนิเวอร์แซลอินดิเคเตอร์ จากสีน้ำตาบเป็นสีเขียวน้ำเงิน
ดินเป็นกลาง จะไม่เปลี่ยนสีกระดาษยูนิเวอร์แซลดิเคเตอร์
ดินเป็นกรด จะเปลี่ยนสีกระดาษยูนิเวอร์แซลอินดิเคเตอร์จากสีน้ำตาลเป็นสีแดง
ดินเป็นเบส จะเปลี่ยนสีกระดาษยูนิเวอร์แซลอินดิเคเตอร์ จากสีน้ำตาบเป็นสีเขียวน้ำเงิน
ดินเป็นกลาง จะไม่เปลี่ยนสีกระดาษยูนิเวอร์แซลดิเคเตอร์
ประโยชน์ของอินดิเคเตอร์
1.ใช้เป็นตัวบอกจุดยุติในการติเตรต
- ถ้าติเตรตกรดแก่ เบสแก่ ใช้อินดิเคเตอร์ที่มีช่วง pH = 7 (เลือกใช้ประมาณ 7 เพราะ จะได้เกลือกลาง)
- ถ้าติเตรตกรดแก่ เบสอ่อน ใช้อินดิเคเตอร์ที่มีช่วง pH < 7 (จะเกิดเกลือกรด)
- ถ้าติเตรตกรดอ่อน เบสแก่ ใช้อินดิเคเตอร์ที่มีช่วง pH > 7 (จะเกิดเกลือเบส)
2. กระดาษลิตมัส ซึ่งมี2 สี คือ กระดาษลิตมัสสีน้ำเงินและสีแดง เมื่อทดสอบกับดินจะเกิดการเปลี่ยนแปลงดังนี้
ดินเป็นกรด จะเปลี่ยนกระดาษลิตมัสสีน้ำเงินเป็นสีแดง แต่สีแดงไม่เปลี่ยนแปลง
ดินเป็นเบส จะเปลี่ยนกระดาษลิตมัสสีน้ำเงินเป็นสีแดง แต่สีแดงไม่เปลี่ยนแปลง
ดินเป็นกลาง จะไม่เปลี่ยนสีกระดาษลิตมัสทั้งสีน้ำเงินและสีแดง
ดินเป็นกรด จะเปลี่ยนกระดาษลิตมัสสีน้ำเงินเป็นสีแดง แต่สีแดงไม่เปลี่ยนแปลง
ดินเป็นเบส จะเปลี่ยนกระดาษลิตมัสสีน้ำเงินเป็นสีแดง แต่สีแดงไม่เปลี่ยนแปลง
ดินเป็นกลาง จะไม่เปลี่ยนสีกระดาษลิตมัสทั้งสีน้ำเงินและสีแดง
ความหมายของช่วง pH ของอินดิเคเตอร์
ช่วง pH ของอินดิเคเตอร์ หมายถึง ช่วง pH ของสารละลายที่อินดิเคเตอร์ค่อย ๆ เปลี่ยนสีจากสีหนึ่งไปยังอีกสีหนึ่ง หรือเป็นส่วน pH ที่อินดิเคเตอร์มีทั้งสีของ HIn และสีของ In- ผสมกัน ในการบอกช่วง pH ของอินดิเคเตอร์ จะต้องกำหนดสีที่เปลี่ยนด้วย เช่น
โบรโมไทมอลบลู ช่วง pH 6.0 – 7.6
การเปลี่ยนสี เหลือง – น้ำเงิน
หมายความว่า ถ้าสารละลายมี pH < 6.0 อินดิเคเตอร์จะให้สีเหลือง ถ้าสารละลายมี pH > 7.6 อินดิเคเตอร์จะให้สีน้ำเงิน และถ้าสารละลายมี pH อยู่ระหว่าง 6.0 – 7.6 อินดิเคเตอร์จะให้สีเขียว ซึ่งเป็นสีผสมของ HIn และ In-
ช่วง pH ของอินดิเคเตอร์ หมายถึง ช่วง pH ของสารละลายที่อินดิเคเตอร์ค่อย ๆ เปลี่ยนสีจากสีหนึ่งไปยังอีกสีหนึ่ง หรือเป็นส่วน pH ที่อินดิเคเตอร์มีทั้งสีของ HIn และสีของ In- ผสมกัน ในการบอกช่วง pH ของอินดิเคเตอร์ จะต้องกำหนดสีที่เปลี่ยนด้วย เช่น
โบรโมไทมอลบลู ช่วง pH 6.0 – 7.6
การเปลี่ยนสี เหลือง – น้ำเงิน
หมายความว่า ถ้าสารละลายมี pH < 6.0 อินดิเคเตอร์จะให้สีเหลือง ถ้าสารละลายมี pH > 7.6 อินดิเคเตอร์จะให้สีน้ำเงิน และถ้าสารละลายมี pH อยู่ระหว่าง 6.0 – 7.6 อินดิเคเตอร์จะให้สีเขียว ซึ่งเป็นสีผสมของ HIn และ In-
การคำนวณเกี่ยวกับอินดิเคเตอร์
HIn (aq) + H2O (l) <-------> H3O+ (aq) + In- (aq)
KHln = [H3O+][ In- ] /[Hln]
[H3O+] = KHln [Hln] / [ In- ]
- log[H3O+] = - logKHln -log[Hln] / [ In- ]
pH = - logKHln -log[Hln] / [ In- ]
รูปกรด ; pH = pKHln – log10
pH = pKHln – 1
รูปเบส ; pH = pKHln + log10
pH = pKHln + 1
pH = pKHln + 1
KHln = [H3O+][ In- ] /[Hln]
[H3O+] = KHln [Hln] / [ In- ]
- log[H3O+] = - logKHln -log[Hln] / [ In- ]
pH = - logKHln -log[Hln] / [ In- ]
รูปกรด ; pH = pKHln – log10
pH = pKHln – 1
รูปเบส ; pH = pKHln + log10
pH = pKHln + 1
pH = pKHln + 1
การเปลี่ยนสีของอินดิเคเตอร์
HIn เป็นสัญลักษณ์ของอินดิเคเตอร์ที่อยู่ในรูปกรด (Acid form)
In- เป็นสัญลักษณ์ของอินดิเคเตอร์ที่อยู่ในรูปเบส (Basic form)
In- เป็นสัญลักษณ์ของอินดิเคเตอร์ที่อยู่ในรูปเบส (Basic form)
ตัวอย่างสีของอินดิเคเตอร์แต่ละชนิด จะเปลี่ยนในช่วง pH ที่ต่างกัน

ตัวอย่างที่ 1 กำหนดช่วง pH ของอินดิเคเตอร์ให้ดังนี้
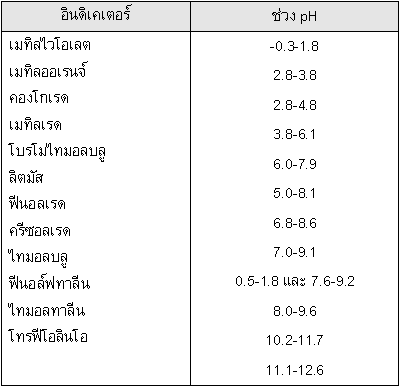
จงเลือกอินดิเคเตอร์ที่เหมาะสมที่สุดในการไทเทรตระหว่างสารละลาย 0.1 โมล/ลิตร HCN จำนวน 50 cm3 กับ 0.1 โมล/ลิตร จำนวน 50 cm3 กำหนดค่า Ka ของกรด HCN = 7.2 x 10-10 ที่ 25 0C และ log 8.4 = 0.92
วิธีทำ
HCN (aq) + NaOH(aq) NaCN (aq) + H2O (l)
NaCN (aq) + H2O (l)
วิธีทำ
HCN (aq) + NaOH(aq)
| เพราะฉะนั้นจำนวนโมลของ HCN = | = 5 x 10-3 โมล | |
| เพราะฉะนั้นจำนวนโมลของ NaOH = | = 5 x 10-3 โมล | |
ดังนั้นสารละลายทั้งสองทำปฏิกิริยากันพอดีด้วยจำนวนโมลเท่ากันได้ผลิตภัณฑ์เป็น NaCN = 5 x 10-3 โมล ในปริมาตร 50 + 50 = 100 cm3
| เพราะฉะนั้น [NaCN] = | x 5 x 10-3 = 0.05 โมล/ลิตร |
NaCN แตกตัวได้ 100 % ดังนี้
NaCN (aq) Na+ (aq) + CN- (aq)
Na+ (aq) + CN- (aq)
0.05 0.05 0.05 โมล/ลิตร
NaCN (aq)
0.05 0.05 0.05 โมล/ลิตร
CN- (aq) + H2O  HCN (aq) + OH- (aq)
HCN (aq) + OH- (aq)
ความเข้มข้นเริ่มต้น 0.05 0 0
ความเข้มข้นที่เปลี่ยนไป -x +x +x
ความเข้มข้นที่ภาวะสมดุล 0.05-x x x

ความเข้มข้นเริ่มต้น 0.05 0 0
ความเข้มข้นที่เปลี่ยนไป -x +x +x
ความเข้มข้นที่ภาวะสมดุล 0.05-x x x

| 1.4 x 10-5 = | ||
| 1.4 x 10-5 = | ( | |
x = 8.4 x 10-4 = [OH-]
pOH = -log[OH-] = -log[8.4 x 10-4] = -0.92 + 4 = 3.08
pH = 14 - pOH = 14 - 3.08 = 10.92
เนื่องจาก pH ของสารละลายหลังไทเทรตเท่ากับ 10.92 ดังนั้นจะต้องเลือกใช้อินดิเคเตอร์ไทมอลทาลีน ซึ่งมีช่วงการเปลี่ยนแปลง pH อยู่ระหว่าง 10.2-11.7 จึงจะเหมาะสมที่สุด
pOH = -log[OH-] = -log[8.4 x 10-4] = -0.92 + 4 = 3.08
pH = 14 - pOH = 14 - 3.08 = 10.92
เนื่องจาก pH ของสารละลายหลังไทเทรตเท่ากับ 10.92 ดังนั้นจะต้องเลือกใช้อินดิเคเตอร์ไทมอลทาลีน ซึ่งมีช่วงการเปลี่ยนแปลง pH อยู่ระหว่าง 10.2-11.7 จึงจะเหมาะสมที่สุด
ตัวอย่างที่ 2 นำสารละลาย HA ซึ่งเป็นกรดอ่อนชนิดหนึ่งปริมาตร 50.00 cm3 ไปไทเทรตกับสารละลายมาตรฐาน NaOH เข้มข้น 0.15 โมล/ลิตร พบว่าเมื่อเติม NaOH ลงไป 12.00 cm3 จะทำให้สารละลายที่ได้มี pH 7 และเมื่อเติม NaOH ลงไป 16.00 cm3 จะถึงจุดยุติพอดี สารละลายกรด HA มีความเข้มข้นเริ่มต้นเท่าใด และการไทเทรตกรด-เบสคู่นี้ควรใช้อินดิเคเตอร์ชนิดใด (กำหนด Ka ของกรดอ่อน HA = 1.7 x 10-6) กำหนดให้
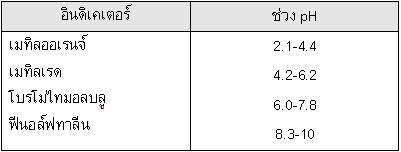
วิธีทำ
ที่จุดยุติจำนวนโมล NaOH = 0.1500 x mol
mol
สมมติความเข้มข้นเริ่มต้นของ HA = X โมล/ลิตร
HA + NaOH NaA + H2O
NaA + H2O
จำนวนโมล HA : NaOH = 1 : 1
เพราะฉะนั้นจำนวนโมล HA = 0.1500 x ด้วย
ด้วย
= X( )
)
X( ) = 0.1500 x
) = 0.1500 x 
X = 0.048
ความเข้มข้นเริ่มต้น = 0.048 โมล/ลิตร
เพราะฉะนั้นความเข้มข้นของ NaA = 0.048 โมล/ลิตร
การไทเทรตกรดอ่อนกับเบสแก่ที่จุดยุติ มี NaA ซึ่งแตกตัวให้ A-
A- (aq) + H2O (l) HA (aq) + OH-(aq)
HA (aq) + OH-(aq)
ความเข้มข้นเริ่มต้น 0.048 0 0
ความเข้มข้นที่เปลี่ยนไป -x +x +x
ความเข้มข้นที่ภาวะสมดุล 0.048-x x x

5.88 x 10-9 =
1.4 x 10-5 = (
( x มีค่าน้อยมาก 0.048-x
x มีค่าน้อยมาก 0.048-x  0.048)
0.048)
x = 1.68 x 10-5 = [OH-]
pOH = -log[OH-] = -log[1.68 x 10-5] = 4.77
pH = 14 - pOH = 14 - 4.77 = 9.22
ดังนั้น ควรใช้ฟีนอล์ฟทาลีนเป็นอินดิเคเตอร์ ที่จุดยุติจำนวนโมล NaOH = 0.1500 x
สมมติความเข้มข้นเริ่มต้นของ HA = X โมล/ลิตร
HA + NaOH
จำนวนโมล HA : NaOH = 1 : 1
เพราะฉะนั้นจำนวนโมล HA = 0.1500 x
= X(
X(
X = 0.048
ความเข้มข้นเริ่มต้น = 0.048 โมล/ลิตร
เพราะฉะนั้นความเข้มข้นของ NaA = 0.048 โมล/ลิตร
การไทเทรตกรดอ่อนกับเบสแก่ที่จุดยุติ มี NaA ซึ่งแตกตัวให้ A-
A- (aq) + H2O (l)
ความเข้มข้นเริ่มต้น 0.048 0 0
ความเข้มข้นที่เปลี่ยนไป -x +x +x
ความเข้มข้นที่ภาวะสมดุล 0.048-x x x

5.88 x 10-9 =
1.4 x 10-5 =
x = 1.68 x 10-5 = [OH-]
pOH = -log[OH-] = -log[1.68 x 10-5] = 4.77
pH = 14 - pOH = 14 - 4.77 = 9.22
การเปลี่ยนสีของ กรด-เบส
